原电池和电解池的区别(原电池和电解池的区别是什么)
大家好,下面小编给大家分享一下。很多人不知道原电池和电解池的区别。以下是详细的解释,现在让我们来看看!
很多朋友对原电池和电解池的区别和联系,原电池和电解池的区别不是很了解,125小编刚好整理了这方面的知识,今天就来带大家一探究竟。

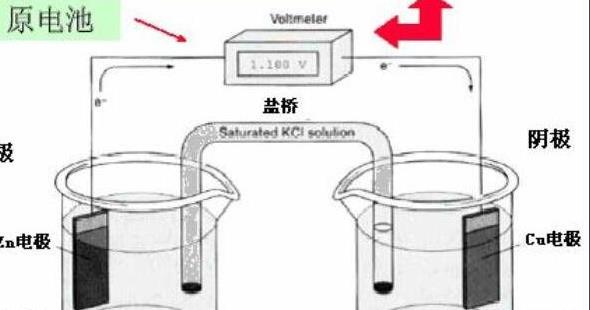
原电池概述通过氧化还原反应产生电流的装置称为原电池,也可以说是将化学能转化为电能的装置。一些原电池可以形成可逆电池,而另一些则不能。当一次电池放电时,负电极经历氧化反应,正电极经历还原反应。比如铜锌一次电池,也叫丹妮尔电池,正极是铜,浸在硫酸铜溶液中;负电极是浸在硫酸锌溶液中的锌板。
两种电解质溶液通过盐桥连接,两个电极通过导线连接形成一次电池。通常使用的干电池是根据原电池的原理制成的。
原电池发明的历史可以追溯到18世纪晚期,当时意大利生物学家伽伐尼正在进行一项著名的青蛙实验。当用金属手术刀接触青蛙腿时,发现青蛙腿会抽搐。著名的伏特认为,这是金属与蛙腿组织液(电解质溶液)之间的电流刺激造成的。1800年,伏特设计了一种叫做伏特反应器的装置,以锌为负极,银为正极,盐水为电解质溶液。
1836年,丹尼尔发明了世界上第一块实用电池,并用于早期的铁路信号灯。
电解槽概述电解槽主要用于高纯度金属的工业生产。它是将电能转化为化学能的装置(由外接电源、电解质溶液、阳极和阴极电极组成)。通过使电流通过电解质溶液或熔融电解质,在阴极和阳极引起氧化还原反应的过程。使电流通过电解质溶液或熔融电解质并在阴极和阳极引起还原和氧化反应的过程称为电解。把电能转化为化学能的装置叫做电解池或电解电池。
当离子到达电极时,它们失去或获得电子,导致氧化还原反应。它耗电。
原电池与电解池的区别1、电解池与原电池的本质区别是电解池将电能转化为化学能;原电池将化学能转化为电能。2、电解槽与原电池装置的区别:电解槽有外接电源;主电池没有外部电源。
3、电解槽与原电池的电子流方向的区别:原电池的电子流方向正好与电流方向相反(电流正流,电子带负电);电解池恰好与原电池的电子流动方向相反(电子通过负极流出进入电解池)。4、电解槽与原电池的应用区别:铅蓄电池使用原电池;电解池用于电镀、精炼和冶金。5、电解槽与原电池级别的区别:电解槽称为阴极和阳极;原电池被称为正极和负极。
6、电解槽与原电池的区别:原电池是外接电源,自发的;电解槽需要通电,是无源的。
以上就是关于原电池和电解池的区别和联系,原电池和电解池的区别的知识,希望能够帮助到大家!
以上解释了原电池和电解池的区别。本文到此结束,希望对大家有所帮助。如果信息有误,请联系我们进行更正。
本网站文章仅供交流学习 ,若来源标注错误或侵犯到您的权益烦请告知,我们将立即删除. 邮箱jdapk@qq.com